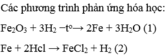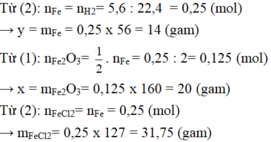Cho 10,2 g hỗn hợp Natri và sắt phản ứng hoàn toàn với nước sau phản ứng thu được 2,128 lít khí ở điều kiện tiêu chuẩn ,biết trong của quá trình thu khí bị hao hụt Mất 5%. Xác định phần trăm mỗi kim loại trong hỗn hợp trên

Những câu hỏi liên quan
Cho 9,3 g hỗn hợp 2 kim loại Natri và Kali tác dụng hoàn toàn với nước dư, thu được 6,72 lít khí H2 ở điều kiện tiêu chuẩn. viết các phương trình phản ứng Tính khối lượng mỗi kim loại
`2Na+2H_2O->2NaOH+H_2`
x-----------------------------`1/2`x mol
`2K+2H_2O->2KOH+H_2`
y---------------------------`1/2` y mol
`n_(H_2)=(6,72)/(22,4)=0,3 mol`
Ta có phương trình :
\(\left\{{}\begin{matrix}23x+39y=9,3\\\dfrac{1}{2}x+\dfrac{1}{2}y=0,3\end{matrix}\right.\)
-> nghiệm vô lí
`#YBTran~`
Đúng 0
Bình luận (0)
Cho 2,24 lít khí CO ở điều kiện tiêu chuẩn từ từ đi qua ống sứ nung nóng được 4 g một oxit sắt đến khi phản ứng xảy ra hoàn toàn khí thu được sau phản ứng có tỉ khối so với Hiđrô bằng 20 xác định công thức của oxit sắt và phần trăm về khối lượng của khí CO2 trong hỗn hợp khí sau phản ứng
Xem chi tiết
Theo gt ta có: $n_{CO}=0,1(mol)$
Bảo toàn nguyên tố C và theo tỉ khối ta có:
$n_{CO}=0,025(mol);n_{CO_2}=0,075(mol)$
Ta lại có: $n_{O/oxit}=n_{CO_2}=0,075(mol)$
Gọi CTTQ của oxit sắt đó là $Fe_xO_y$
Ta có: $M_{Fe_xO_y}=\frac{160y}{3}$
Do đó công thức của oxit sắt là $Fe_3O_4$
Đúng 1
Bình luận (0)
Dùng v lít khí H2 khử hoàn toàn hỗn hợp đồng 2 oxit và sắt 3 oxit ở nhiệt độ thích hợp sau phản ứng thu được 24 g hỗn hợp gồm hai kim loại trong đó có 12 gam Cu Viết các phương trình phản ứng xảy ra tính V ở điều kiện tiêu chuẩn
\(m_{Cu}=12g\Rightarrow n_{Cu}=\dfrac{12}{64}=0,1875mol\)
\(\Rightarrow m_{Fe}=m_{kl}-m_{Cu}=24-12=12g\Rightarrow n_{Fe}=\dfrac{3}{14}mol\)
\(CuO+H_2\rightarrow Cu+H_2O\)
\(\dfrac{12}{64}\) \(\dfrac{12}{64}\)
\(Fe_2O_3+3H_2\rightarrow2Fe+3H_2O\)
\(\dfrac{9}{28}\) \(\dfrac{3}{14}\)
\(\Rightarrow\Sigma n_{H_2}=\dfrac{12}{64}+\dfrac{9}{28}=\dfrac{57}{112}mol\)
\(\Rightarrow V_{H_2}=\dfrac{57}{112}\cdot22,4=11,4l\)
Đúng 3
Bình luận (0)
Dùng khí hiđro dư để khử x gam sắt(III) oxit, sau phản ứng người ta thu được y gam sắt kim loại. Nếu dùng lượng sắt này cho phản ứng hoàn toàn với axit clohiđric có dư thì thu được 5,6 lít khí hiđro đo ở điều kiện tiêu chuẩn.
a) Viết các phương trình phản ứng hóa học.
b) Hãy xác định giá trị x, y và lượng muối sắt(II) clorua tạo thành sau phản ứng.
Hòa tan 9g hóa học kim loại gồm Cu và Zn trong dung dịch HCL. Phản ứng xảy ra hoàn toàn thu được 896ml khí H2 ở điều kiện tiêu chuẩn, xác định thành phần phần trăm và khối lượng của kim loại trong hỗn hợp ban đầu.
PT: \(Zn+2HCl\rightarrow ZnCl_2+H_2\)
Ta có: \(n_{H_2}=\dfrac{0,896}{22,4}=0,04\left(mol\right)\)
Theo PT: \(n_{Zn}=n_{H_2}=0,04\left(mol\right)\Rightarrow m_{Zn}=0,04.65=2,6\left(g\right)\)
⇒ mCu = 9 - 2,6 = 6,4 (g)
\(\Rightarrow\left\{{}\begin{matrix}\%m_{Zn}=\dfrac{2,6}{9}.100\%\approx28,89\%\\\%m_{Cu}\approx71,11\%\end{matrix}\right.\)
Đúng 1
Bình luận (0)
Cho 20,16 lít khí CO phản ứng với một lượng oxit MxOy nung nóng. Sau khi phản ứng xảy ra hoàn toàn, thu được 25,2 gam kim loại M và hỗn hợp khí X. Cho toàn bộ lượng hỗn hợp khí X qua bình chứa dung dịch Ca(OH)2 dư tạo ra m gam kết tủa và có 6,72 lít khí thoát ra. Hòa tan hoàn toàn lượng kim loại trên trong dung dịch HCl dư, thấy thoát ra 10,08 lít khí H2. Xác định công thức oxit và tính m. Biết thể tích các khí đo ở điều kiện tiêu chuẩn.
Đọc tiếp
Cho 20,16 lít khí CO phản ứng với một lượng oxit MxOy nung nóng. Sau khi phản ứng xảy ra hoàn toàn, thu được 25,2 gam kim loại M và hỗn hợp khí X. Cho toàn bộ lượng hỗn hợp khí X qua bình chứa dung dịch Ca(OH)2 dư tạo ra m gam kết tủa và có 6,72 lít khí thoát ra. Hòa tan hoàn toàn lượng kim loại trên trong dung dịch HCl dư, thấy thoát ra 10,08 lít khí H2. Xác định công thức oxit và tính m. Biết thể tích các khí đo ở điều kiện tiêu chuẩn.
Dung dịch Ca(OH)2 không hấp thụ khí CO nên 6,72 lít khí thoát ra chính là khí CO dư.

Đúng 0
Bình luận (0)
Hoàn tan hoàn toàn 8,8 gam hỗn hợp hai kim loại kiềm thổ (nhóm 2A ) ở hai chu kì liên tiếp vào dung dịch HCL .Sau phản ứng thu được 6.72 lít khí ở điều kiện tiêu chuẩn a) hãy xác định hai lim loại ( cho Be9;Mg24;Ca40;Sr87;Ba137)b) tính phần trăm khối lượng của chúng trong mỗi hỗn hợp c)tính nồng độ mol/l của muối thu được sau phản ứng
Đọc tiếp
Hoàn tan hoàn toàn 8,8 gam hỗn hợp hai kim loại kiềm thổ (nhóm 2A ) ở hai chu kì liên tiếp vào dung dịch HCL .Sau phản ứng thu được 6.72 lít khí ở điều kiện tiêu chuẩn
a) hãy xác định hai lim loại ( cho Be=9;Mg=24;Ca=40;Sr=87;Ba=137)
b) tính phần trăm khối lượng của chúng trong mỗi hỗn hợp
c)tính nồng độ mol/l của muối thu được sau phản ứng
a gọi công thức chung của 2 KL là M
M+ 2HCl => MCl2 + H2
0,3 <= 0,3
=> M = 8,8/ 0,3 = 29,33
mà 2 kim loại thuộc 2 chu kì liên tiếp = > Mg và Ca
b
24x + 40y = 8,8
x + y = 0,3
=> x= 0,2 y = 0,1
% Mg = 54.54% %Ca = 45,46%
câu c hình như cần phải có Vdd nữa bạn ơi~~~~~
Đúng 0
Bình luận (0)
Cho 3,68 gam hỗn hợp sắt và magie phản ứng hoàn toàn với dung dịch HNO3 đặc, nóng thu được 5,376 lít khí NO2 duy nhất (đktc). Xác định thành phần phần trăm khối lượng mỗi kim loại trong hỗn hợp và tính khối lượng axit đã phản ứng.
\(3,68g\left\{{}\begin{matrix}Fe\\Mg\end{matrix}\right.+HNO3->\left\{{}\begin{matrix}Fe\left(NO3\right)3\\Mg\left(NO3\right)2\end{matrix}\right.+5,376\left(l\right)NO2\)
Bảo toàn e :
\(3x+2y=0,24\)
Ta có :
\(\left\{{}\begin{matrix}56x+24y=3,68\\3x+2y=0,24\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}x=0,04\left(mol\right)\\y=0,06\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}\%mFe=\dfrac{0,04.56}{3,68}=60,87\%\\\%mMg=\dfrac{0,06.24}{3,68}=39,13\%\end{matrix}\right.\)
Bảo toàn nguyên tố Fe và Mg :
\(nFe=nFe\left(NO3\right)3=0,04\left(mol\right)\)
\(nMg=nMg\left(NO3\right)2=0,06\left(mol\right)\)
Ta có : \(nHNO3pu=0,04.3+0,06.2=0,24\left(mol\right)\)
\(\Rightarrow mHNO3=0,24.63=15,12\left(g\right)\)
Đúng 1
Bình luận (2)
Tiến hành phản ứng nhiệt nhôm với Fe2O3 trong điều kiện không có không khí. Chia hỗn hợp sau phản ứng thành hai phần. Phần một có khối lượng 67 gam cho tác dụng với lượng dư dung dịch NaOH thấy có 16,8 lít H2 bay ra. Hòa tan phần hai bằng một lượng dư dung dịch HCl thấy có 84 lít H2 bay ra. Biết các phản ứng xảy ra hoàn toàn và các thể tích khí đo ở điều kiện tiêu chuẩn. Khối lượng Fe thu được trong quá trình nhiệt nhôm là A. 112 B. 84 C. 168 D. 56
Đọc tiếp
Tiến hành phản ứng nhiệt nhôm với Fe2O3 trong điều kiện không có không khí. Chia hỗn hợp sau phản ứng thành hai phần. Phần một có khối lượng 67 gam cho tác dụng với lượng dư dung dịch NaOH thấy có 16,8 lít H2 bay ra. Hòa tan phần hai bằng một lượng dư dung dịch HCl thấy có 84 lít H2 bay ra. Biết các phản ứng xảy ra hoàn toàn và các thể tích khí đo ở điều kiện tiêu chuẩn. Khối lượng Fe thu được trong quá trình nhiệt nhôm là
A. 112
B. 84
C. 168
D. 56
Đáp án A
Hỗn hợp rắn gồm Al, Al2O3, Fe với n Fe = 2 n Al 2 O 3 . Chia thành 2 phần không bằng nhau:
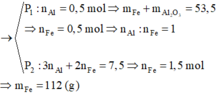
Đúng 0
Bình luận (0)